





| 编号 | 258 |
| 总例数 | 31例 |
| 性别例数 | 男24例,女7例 |
| 治疗组例数 | 16例 |
| 对照组例数 | 15例 |
| 年龄区间 | 治疗组62~81岁;对照组60~82岁 |
| 平均年龄 | 治疗组(71±6)岁;对照组(72±8)岁 |
| 疾病 | 2型糖尿病 |
| 并发症 | |
| 药品通用名称 | 生物合成人胰岛素 |
| 药品商品名称 | 诺和灵R |
| 药品英文名称 | Biosynthetic Human Insulin |
| 剂型 | 注射剂 |
| 规格 | |
| 批准文号 | |
| 生产厂家 | |
| 分类 | 生物制品 |
| 用药目的 | 治疗 |
| 用法用量 | CSⅡ组,采用美敦力公司Minimed 508C型胰岛素泵,连续给予短效胰岛素(诺和灵R)基础用量,以患者实际体重×0.44得到患者每日所需胰岛素量,其中50%作为每日基础率设置成4~24时段的不同量持续经皮下泵入,另外50%平均分配到3餐前给予,根据血糖情况酌情调整基础及餐前剂量。MSⅡ组于3餐前皮下注射诺和灵R,睡前注射中效胰岛素(诺和灵N)。两组患者均治疗3个月。使用美国强生公司One Touch血糖仪检测血糖。治疗初始每天测3餐前、3餐后2小时及睡前22:00和凌晨3:00共8次血糖,血糖达标连续 |
| 联合用药 | |
| 疗效评价标准 | 血糖控制目标:餐前血糖<6.1mmol/L,餐后2小时血糖<7.8mmol/L。 |
| 治疗效果及临床指征比较 |
两组各项指标检测结果:1个月治疗期内两组患者经胰岛素强化治疗后均基本达到血糖控制目标,CSⅡ组患者各时段血糖、血糖达标时间和胰岛素用量均优于注射治疗组,胰岛素分泌指数CSⅡ组优于MSⅡ组,但差异无统计学意义,见表1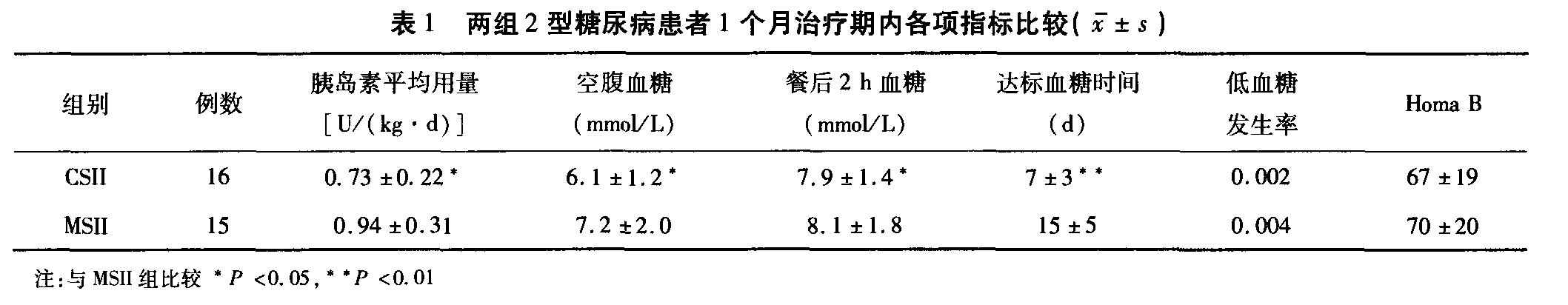 。HbAlc、胰岛素用量和Homa B比较:治疗3个月后CSⅡ组HbAlc低于MSⅡ组,但差异无统计学意义,胰岛素用量显著低于MSⅡ组,两组Homa B均较治疗1个月时明显增加,见表2  。 |
| 本研究报道不良反应 | 1个月治疗期内两组患者低血糖反应程度均较轻,多为血糖监测发现的无明显自觉症状的低血糖,未出现低血糖昏迷症状者。但CSⅡ组低血糖发生率显著少于MSⅡ组(0.002和0.004,P<0.05)。在治疗观察中,发现与胰岛素泵有关或可能相关的不良事件中主要是需24小时配戴胰岛素泵有患者感到不便。此外,患者还有硬结、红斑、皮疹和荨麻疹以及局部皮肤红肿,甚至化脓等皮肤过敏反应。 |
| 其他报道不良反应 |