
二、氧化剂与还原剂的共轭关系
在氧化还原反应中,还原剂被氧 化,生成与之共轭的氧化剂。

同理,在氧化还原反应中,氧化剂被还原,生成与之共轭的还原剂。
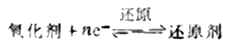
因此,氧化剂与还原剂的共轭关系可用下式表示:

一种还原剂要失去电子表现出可被氧化的性质,只有在能得到电子可被还原的另一种氧化剂的存在下才能实现,即
 例如,在 Zn +Cu2+=Cu+Zn2+反应中,还原剂1Z失去电子,氧化数升高,其产物为氧化化剂1Zn2+;氧化剂2Cu2+得到电子,氧化数降低,其产物为还原剂2Cu。这样Zn与Zn2+,Cu2+与 Cu构成了如下两个共轭的氧化还原电对:
例如,在 Zn +Cu2+=Cu+Zn2+反应中,还原剂1Z失去电子,氧化数升高,其产物为氧化化剂1Zn2+;氧化剂2Cu2+得到电子,氧化数降低,其产物为还原剂2Cu。这样Zn与Zn2+,Cu2+与 Cu构成了如下两个共轭的氧化还原电对:
Zn2+/Zn Cu2+/Cu
(氧化剂)(还原剂) (氧化剂)(还原剂)
在氧化还原电对中,氧化数高的物质为氧化型物质,氧化数低的物质为还原型物质。如果还原剂越强(失去电子的能力越大),则其共轭的氧化剂越弱(得到电子的能力越小);如果氧化剂越强,则其共轭的还原剂越弱。例如,在MnO-4/Mn2+电对中,MnO4是一个强氧化剂,Mn2+是一个弱还原剂。氧化还原反应是按较强的氧化剂和较强的还原剂相互作用方向进行的。医学 全在.线提供